FAQ sur la terminologie et les procédures de FIV
Quels sont les termes les plus courants à connaître en matière de FIV ?
Parmi les étapes essentielles figurent la stimulation ovarienne, la ponction ovocytaire, la fécondation, le transfert embryonnaire et l’implantation. Les comprendre permet d’aborder le traitement plus sereinement et en toute confiance.
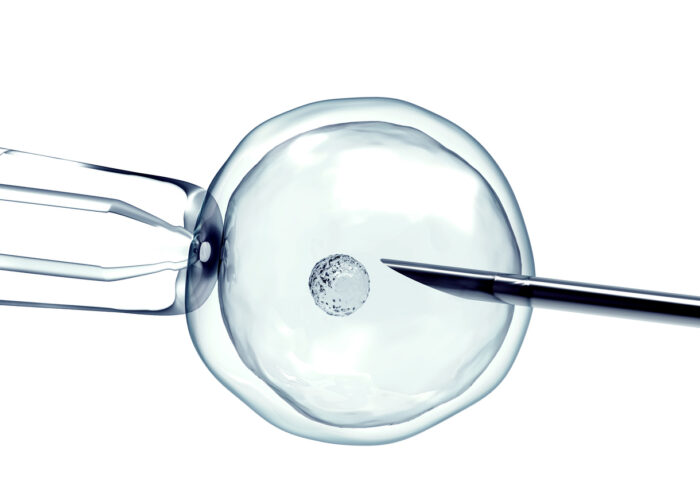
Quelle est la différence entre FIV et ICSI ?
La FIV classique prévoit la mise en contact des ovocytes et des spermatozoïdes pour que la fécondation se fasse spontanément. Avec l’ICSI (injection intracytoplasmique de spermatozoïde), un spermatozoïde est directement injecté dans un ovocyte. Cette technique est souvent proposée en cas d’infertilité masculine.
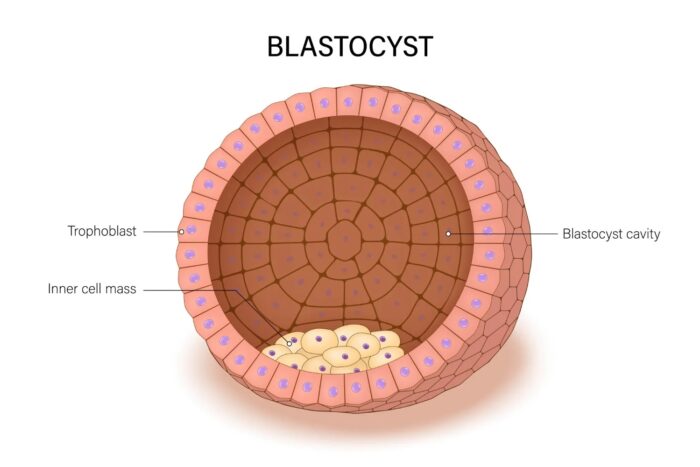
Que signifie DPI ? Et PGT ?
En France, on parle de DPI (diagnostic préimplantatoire). Dans les pays anglophones et dans certaines publications médicales, on retrouve aussi le sigle PGT (preimplantation genetic testing). Il s’agit d’un examen réalisé sur les embryons avant leur transfert, afin de détecter des anomalies chromosomiques ou certaines maladies génétiques monogéniques. L’objectif est d’aider à sélectionner les embryons ayant les meilleures chances de donner une grossesse évolutive.
Combien d’embryons sont généralement transférés lors d’une FIV ?
Le plus souvent, en particulier chez les femmes jeunes ou lorsque les embryons ont été testés ou proviennent d’un don d’ovocytes, un seul embryon est transféré afin de réduire le risque de grossesse multiple. Votre médecin vous conseillera en fonction de votre situation.
Qu’est-ce qu’un transfert d’embryon congelé (TEC) ?
Le transfert d’embryon congelé correspond à la décongélation d’un embryon vitrifié lors d’un cycle précédent, puis à son transfert dans l’utérus. Cela permet une meilleure organisation et un timing plus adapté.
La FIV garantit-elle une grossesse ?
Non, aucun traitement ne peut garantir une grossesse. La FIV augmente considérablement les chances, mais le succès dépend de plusieurs facteurs comme l’âge, la qualité des embryons et l’état de santé général.
La FIV est-elle douloureuse ?
La FIV implique des injections, des examens de suivi et quelques gestes médicaux. Certaines femmes ressentent de légers inconforts, mais la plupart trouvent le processus tout à fait supportable. L’équipe de Procriar vous accompagne tout au long du parcours.
Quand envisager un diagnostic préimplantatoire (DPI/PGT) ?
Le DPI peut être recommandé après 37 ans, en cas de fausses couches à répétition, de maladie génétique connue ou d’échecs répétés de FIV.
Combien de temps dure un cycle complet de FIV ?
Un cycle complet de FIV dure généralement entre 6 et 8 semaines, du début de la stimulation ovarienne jusqu’au test de grossesse. La durée peut toutefois varier en fonction du protocole personnalisé.
Conclusion
Mieux comprendre la terminologie et les étapes de la FIV permet d’aborder son parcours de PMA avec plus de sérénité et de confiance.
Chez Procriar, nous vous accompagnons avec expertise, disponibilité et bienveillance. Si vous avez des questions sur la FIV ou si vous souhaitez échanger avec l’un de nos médecins ou spécialistes, n’hésitez pas à nous contacter. Nous sommes là pour vous soutenir à chaque étape.